
O nitrogênio (N2) é um gás que ocupa 80% da atmosfera terrestre. É portanto extremamente abundante. Do ponto de vista da ecologia é curioso que as plantas não possam utilizar estes gás para suprir suas necessidades de nitrogênio.
=======
Sabemos que as plantas fazem fotossíntese para produzir glicose que lhes serve como fonte de energia e material estrutural, como a celulose (que é um polímero de glicose). No entanto, para fabricar proteínas e DNA (ou RNA) a planta necessita nitrogênio. Especialmente plantas como o feijão ou a soja que apresentam níveis mais altos de proteínas.
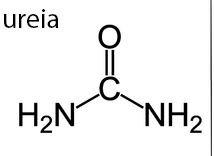
Ureia é um dos fertilizantes que fornecem nitrogênio ao solo:
==============
A ligação química entre os 2 átomos de nitrogênio na molécula N2 é tripla. Ela é muito forte. Por isso é difícil quebrá-la para formar substâncias nitrogenadas que podem ser assimiladas pelas plantas. As plantas absorvem o nitrogênio na forma de NO3 (nitrato).
==========
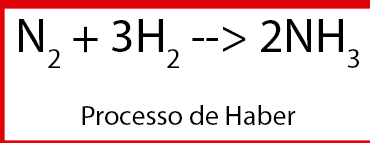
Humanos apenas conseguiram produzir nitratos a partir de nitrogênio do ar, em grandes quantidades, na época da segunda guerra mundial. Nitratos eram produzidos pelos alemães para a manufatura de explosivos, pois havia um bloqueio comercial que impedia a entrada de minérios contendo nitratos no país. Hoje em dia o processo de Haber é usado para a produção de fertilizantes e também de explosivos. Ele consiste no aquecimento de hidrogênio e nitrogênio a altas pressões, usando o ferro como catalisador.
As bactérias fixam o nitrogênio a temperaturas e pressões muito mais baixas. Para isso usam um catalisador (neste caso uma enzima pois trata-se de bioquímica) que também contém ferro, além de outros metais como o molibdênio.
Desastres envolvendo explosões envolvendo nitratos
O nitrato de amônio é explosivo pois é uma substância que contém ambos oxidante (nitrato) e combustível (amônio).
No estado americano do Texas houve 2 explosões acidentais de nitrato de amônio famosas : a explosão de um navio carregado com o produto em um porto do Texas, onde morreram 581 pessoas e mais de mil prédios foram destruídos e a explosão de um depósito do produto, a qual é explicada em detalhes em um excelente vídeo com animações (é em inglês portanto sugiro incluir as legendas-em inglês pois não tem em português- para auxiliar na compreensão)
==========
Ciclo do nitrogênio
Bactérias convertem o N2 em amônia (NH3), também chamada de amoníaco. Devido à presença de água no solo, a amônia é convertida em NH4 (íons de amônio). Este passo é muito importante, pois a amônia é tóxica para as plantas e animais. Além disso, a amônia é um gás que seria perdido de volta para a atmosfera.
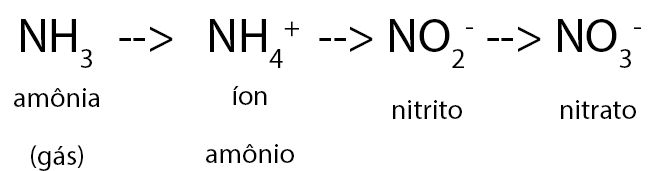
Outras bactérias convertem a amônia em nitrito (NO2). As bactérias que fazem esta conversão são do gênero Nitrosomonas e portanto este processo é chamada de nitrosação.
Finalmente outro gênero de bactérias faz a conversão dos nitritos em nitratos, que são as substâncias absorvidas pelas plantas. Este processo é chamado de nitratação.
O processo de nitrificação é a conversão de amônia em nitratos. O processo de conversão de N2 em amônia é a fixação do nitrogênio. Existem também as bactérias que fazem a desnitrificação, que é o trajeto oposto: é a conversão de nitratos em N2.
Ver: ENEM 2017 - Questão 96- ciclo do nitrogênio